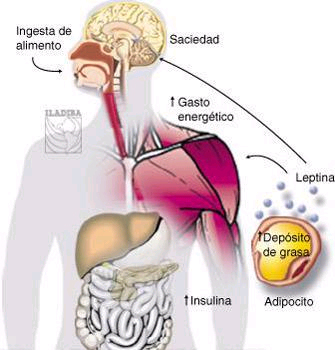
Indivíduos apresentando redução de peso ou deficiência de leptina possuem um menor gasto energético combinado a uma maior sensação de fome e/ ou saciedade atrasada,em comparação com indivíduos sem redução de peso. Devido ao fato de que a leptina exógena inibe a alimentação em humanos com deficiência congênita de leptina, a sinalização reduzida de leptina pode diminuir a expressão do controle da ingestão alimentar em seres humanos. Este estudo objetivou-se a testar a hipótese de que a redução da sinalização da leptina pode reduzir a expressão de saciedade em seres humanos, através da examinação dos efeitos da reposição da leptina sobre o comportamento alimentar após a perda de peso. Assim, dez indivíduos obesos (4 homens, 6 mulheres) participaram deste estudo e, hospitalizados, receberam a administração de uma fórmula líquida para manutenção de peso. A saciedade foi estudada através da mensuração da ingestão e classificações das disposições de apetite, relacionados 3 horas após a ingestão de 300 kcal da fórmula líquida. Os participantes foram estudados em cada um dos períodos de tempo de 3 horas: 1) enquanto mantiveram o seu peso usual (P inicial) e, em seguida, após a redução de peso e estabilização de 10% abaixo do peso inicial e enquanto receberam 5 semanas da fórmula ou placebo; 2) duas vezes ao dia quando receberam a administração de injecções de placebo (Pi-10% para o placebo); ou 3) “doses de reposição” de leptina (Pi-10% de leptina) em um estudo cruzado duplo-cego com um período de 2 semanas entre os tratamentos. O gasto energético também foi medido em cada período de estudo. Foi encontrado que tanto o gasto de energia e a pontuação na escala analógica visual que refletem saciedade foram significantemente menores nos participantes recebendoplacebo Pi-10%, do que aqueles do grupo 1 e 2. Os autores concluem que os resultados são consistentes com a hipótese de que a ausência de sinalização da leptina após a perda de peso podem atenuar a expressão da inibição da alimentação em seres humanos.
Referência bibliográfica:
KISSILEFF, H.R.; THORNTON, J.C.; TORRES, M.I.; et al. Leptin reverses declines in satiation in weight-reduced obese humans. Am J Clin Nutr; 95: 2 309-317, 2012.