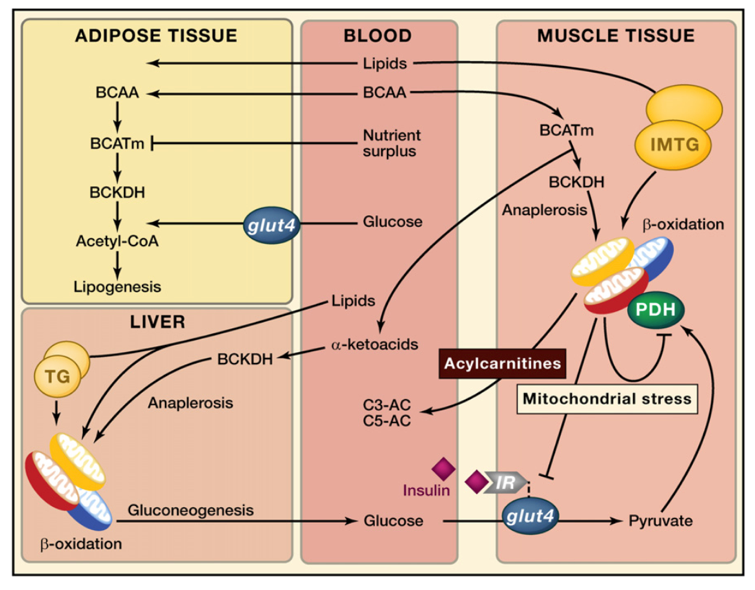
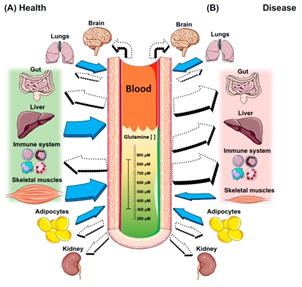
A influência da ingestão/suplementação de aminoácidos no desenvolvimento de fadiga tem sido estudada e discutida desde os anos 80-90 a partir de observações descrevendo que a concentração plasmática de glutamina, bem como a relação glutamato/glutamina, é reduzida em atletas expostos a altos volumes de treinamento (Coutts et al, 2007; Jin et al, 2009; Kingsbury et al, 1998). Sabe-se que a glutamina é o aminoácido glicogênico mais abundante no corpo humano (20% do pool total de aminoácidos sanguíneos) com influência significativa na anaplerose e gliconeogênese (Bassini-Cameron et al, 2008; Curi et al, 2005). Em humanos adultos (em jejum) a concentração plasmática de glutamina é de aproximadamente 550-750 mmol/L e a concentração intramuscular é de 20 mmol/kg de peso úmido (Bowtell et al, 1999). O músculo esquelético é o principal tecido envolvido na síntese de glutamina e é conhecido por liberar glutamina na circulação na faixa de 50 mmol/h no estado pós-prandial (Jonnalagadda, 2007). Por meio da ativação da enzima glicogênio sintetase, a glutamina é considerada um aminoácido potencial para estimular a síntese de glicogênio (Bowtell et al, 1999; Varnier et al, 1995). Além disso, a glutamina é o principal aminoácido carreador de amônia não-tóxico (Bassini-Cameron et al, 2008) e tem papel antioxidante por meio da síntese de glutationa, o que pode contribuir para atenuação do dano muscular (Leite et al, 2016; Raizel et al, 2016).
Nutricionalmente, a glutamina é classificada como aminoácido condicionalmente essencial uma vez que em situações catabólicas (traumas, queimaduras, sepse e exercícios de alta intensidade ou longa duração), a síntese endógena de glutamina pode não ser suficiente para suprir a demanda gerada pela condição fisiológica/patológica gerando, consequentemente, deficiência (Castell et al, 2001; Castell et al, 2002). No tocante ao estímulo mecânico, exercícios de alta intensidade e curta duração aumentam a liberação de glutamina do músculo esquelético para a circulação (Sewell et al, 1994). Já atividades de intensidade baixa/moderada e longa duração, há o influxo do plasma para o músculo esquelético uma vez que síntese tecidual não se faz suficiente para atender a demanda metabólica (Castell et al, 1996; Kingsbury et al, 1998; Varnier et al, 1995).
Inicialmente, a suplementação de glutamina foi estudada principalmente devido ao seu potencial imunomodulador. A diminuição da disponibilidade de glutamina está relacionada com distúrbios no sistema imunológico e aumento na incidência de infecções, principalmente do trato respiratório (Castell et al, 2001). Dos Santos et al. (2009) observaram, em modelo experimental (ratos), que o exercício exaustivo induz um aumento na funcionalidade de macrófagos e aumento no consumo de glutamina nestas células, indicando a importância da glutamina no período pós-treino. Embora seja um estudo conduzido em modelo animal, essa evidência preliminar sugere uma possível aplicação da suplementação de glutamina em indivíduos envolvidos em exercícios exaustivos. Em humanos, a glutamina demonstrou influenciar a proliferação de linfócitos in vitro de modo dose-dependente, sendo a maior taxa de proliferação em uma concentração 600 mmol/L de glutamina (Parry-Billings et al, 1990a). A demanda de glutamina gerada tanto para o fornecimento de energia celular quanto para a síntese de nucleotídeos nas células do sistema imunológico, leva a hipótese que a diminuição no nível plasmático abaixo de 600 mmol/L pode levar efeitos deletérios sobre a função imunológica. Ainda, é possível que o não fornecimento de glutamina pelo músculo esquelético pode resultar na menor proliferação de linfócitos em resposta a antígenos e, portanto, prejudicar a defesa imunológica contra infecções virais. O exercício físico intenso pode diminuir a taxa de liberação de glutamina do músculo esquelético e/ou aumentar a taxa de captação de glutamina por outros órgãos ou tecidos que utilizam glutamina (por exemplo, fígado, rins), limitando a disponibilidade de glutamina para as células do sistema imunológico (Parry-Billings et al, 1990b). Em outras palavras, essa é uma das formas pela qual o exercício de alta demanda pode aumentar o risco imunológico.
Alguns estudos avaliaram a eficácia da suplementação com glutamina sobre a função imune em modelos de treinamento em humanos. De modo randomizado, crossover e controlado por placebo, Rohde et al. (1998) submeteram voluntários saudáveis a 3 sessões seguidas de exercício em cicloergômetro a uma intensidade de 75% VO2max com duração de 60, 45 e 30 minutos cada e intervalo de repouso de 2 horas entre cada sessão. Os indivíduos foram suplementados com 0,1 g/kg de glutamina 30 min antes do final e 30 min após cada sessão de exercício. A concentração de glutamina no plasma declinou de 508 ± 35 mmol/L para 402 ± 38 mmol/L 2 horas após a última sessão de exercício no grupo placebo e foi mantida acima dos níveis de pré-exercício no grupo suplementado. Embora a ingestão de glutamina tenha impedido a queda na concentração plasmática de glutamina, ela não evitou a queda na proliferação de linfócitos 2 horas após a última sessão de exercício. Usando protocolos similares de suplementação com glutamina, outros estudos também demostraram que a suplementação foi capaz prevenir qualquer queda na concentração plasmática de glutamina durante e após 2 horas de exercício e não impediu a diminuição da atividade das células natural killer (20) ou a concentração salivar de imunoglobulina A (Krzywkowski et al, 2001). No estudo de Walsh et al. (2000), os voluntários consumiram 3g de glutamina a cada 15 minutos durante os 30 minutos finais de uma sessão de exercício com duração de 2 horas e a cada 15 minutos durante o período de recuperação de 2 horas (ingestão total de 30g) sem qualquer efeito sobre a diminuição transitória na degranulação de neutrófilos estimulada por bactérias induzida pelo exercício.
Existe uma evidência relatando que a concentração plasmática de bicarbonato foi aumentada em 10% acima do valor basal 90 minutos após a ingestão oral de 2g de glutamina (Welbourne, 1995). No entanto, um estudo controlado por placebo que investigou os efeitos da suplementação de glutamina (30mg /kg) sobre a capacidade de tamponamento extracelular e desempenho em exercício de alta intensidade não encontrou nenhum efeito benéfico sobre o equilíbrio ácido-base ou tempo de exaustão (Haub et al, 1998). Sabe-se também que a suplementação é questionada quanto aos efeitos periféricos uma vez que boa parte da glutamina consumida é retida no trato gastrointestinal como substrato para os enterócitos. Contudo, há evidências que indicam que a glutamina plasmática sofre aumento em resposta a ingestão oral de glutamina (Maughan, 1999). Além disso, doses de 20 a 30g de glutamina são seguras e toleradas em humanos (Gleeson, 2008).
Referências Bibliográficas:
Bassini-Cameron A, Monteiro A, Gomes A, Werneck-de-Castro J, Cameron L. Glutamine protects against increases in blood ammonia in football players in an exercise intensity-dependent way. Br J Sport Med 2008; 42: 260–266. / Bowtell J, Gelly K, Jackman M, Patel A, Simeone M, Rennie M. / Effect of oral glutamine on whole body carbohydrate storage during recovery from exhaustive exercise. J Appl Physiol 1999; 86: 1770–1777. / Castell L, Poortmans J, Newsholme E. Does glutamine have a role in reducing infections in athletes? Eur J Appl Physiol 1996; 73: 488–490. / Castell L, Newsholme E. The relation between glutamine and the immunodepression observed in exercise. Amino Acids 2001; 20: 49–61. / Castell L. Can glutamine modify the apparent immunodepression observed after prolonged, exhaustive exercise? Nutrition 2002; 18: 371–375. / Coutts A, Reaburn P, Piva T, Murphy A. Changes in selected biochemical, muscular strength, power, and endurance measures during deliberate overreaching and tapering in rugby league players. Int J Sports Med 2007; 28: 116–124. / Curi R, Lagranha C.J, Doi SQ, Sellitti DF, Procopio J, Pithon-Curi TC, Corless M, Newsholme P. Molecular mechanisms of glutamine action. J Cell Physiol 2005; 204: 392–401. / Dos Santos R, Caperuto E, Mello M, Rosa L. Effect of exercise on glutamine metabolism in macrophages of trained rats. Eur J Appl Physiol 2009; 107: 309–315. / Jin G, Kataoka Y, Tanaka M, Mizuma H, Nozaki S, Tahara T, Mizuno K, Yamato M, Watanabe Y. Changes in plasma and tissue amino acid levels in an animal model of complex fatigue. Nutrition 2009; 25: 597–607. / Jonnalagadda SS. Glutamine. In: Driskell JA, editor. Sports nutrition: fats and proteins. Boca Raton (FL): CRC Press; 2007. p. 261–77. / Kingsbury K, Kay L, Hjelm M. Contrasting plasma free amino acid patterns in elite athletes: Association with fatigue and infection. Br J Sports Med 1998; 32: 25–33. / Krzywkowski K, Petersen EW, Ostrowski K, Link-Amster H, Boza J, Halkjaer-Kristensen J, Pedersen BK. Effect of glutamine and protein supplementation on exercise-induced decreases in salivary IgA. J Appl Physiol 2001 ; 91: 832–8. / Gleeson M. Dosing and efficacy of glutamine supplementation in human exercise and sport training. J Nutr 2008; 138: 2045–2049. / Leite J, Raizel R, Hypo?lito T, Rosa T, Cruzat V, Tirapegui J. L-glutamine and L-alanine supplementation increase glutamine-glutathione axis and muscle HSP-27 in rats trained using a progressive high-intensity resistance exercise. Appl Physiol Nutr Metab 2016; 41:842–849. / Maughan R. Nutritional ergogenic aids and exercise performance. Nutr Res Rev 1999; 12: 255–280. / Parry-Billings M, Evans J, Calder PC, Newsholme EA. Does glutamine contribute to immunosuppression after major burns? The Lancet 1990a; 336: 523–5. / Parry-Billings M, Blomstrand E, McAndrew N, Newsholme EA. A communicational link between skeletal muscle, brain, and cells of the immune system. Int J Sports Med 1990b; 11 Suppl 2: S122–8. / Raizel R, Leite JSM, Hypo?lito TM, Coqueiro AY, Newsholme P, Cruzat VF, Tirapegui J. Determination of the anti-inflammatory and cytoprotective effects of l-glutamine and l-alanine, or dipeptide, supplementation in rats submitted to resistance exercise. Br J Nutr 2016; 116: 470–479. / Rohde T, MacLean DA, Pedersen BK. Effect of glutamine supplementation on changes in the immune system induced by repeated exercise. Med Sci Sports Exerc 1998; 30: 856–62. / Sewell D, Gleeson M, Blannin A. Hyperammonaemia in relation to high-intensity exercise duration in man. Eur. J. Appl. Physiol. 1994, 69, 350–354. / Varnier M, Leese G, Thompson J, Rennie M. Stimulatory effect of glutamine on glycogen accumulation in human skeletal muscle. Am J Physiol 1995; 269: E309–E315. / Walsh NP, Blannin AK, Bishop NC ,Robson PJ ,Gleeson M. Effect of oral glutamine supplementation on human neutrophil lipopolysaccharide- stimulated degranulation following prolonged exercise. Int J Sport Nutr 2000; 10: 39–50. / Welbourne TC. Increased plasma bicarbonate and growth hormone after an oral glutamine load. Am J Clin Nutr 1995; 61: 1058–61.
Fonte: Vifatorscience